컴퓨터로 사진을 클릭해서 원본을 보시면 더 선명한 화질로 보실 수 있습니다
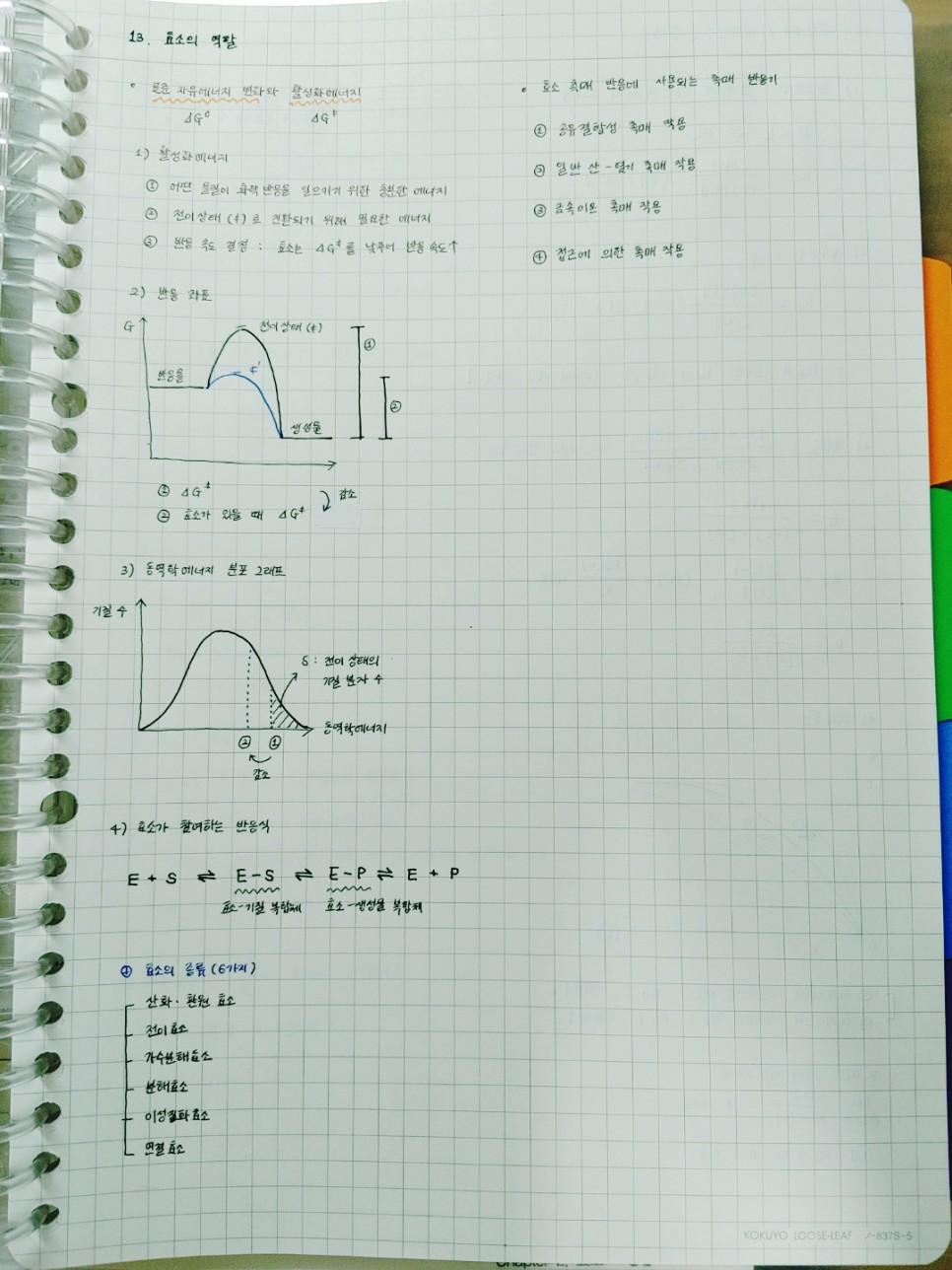
- 효소
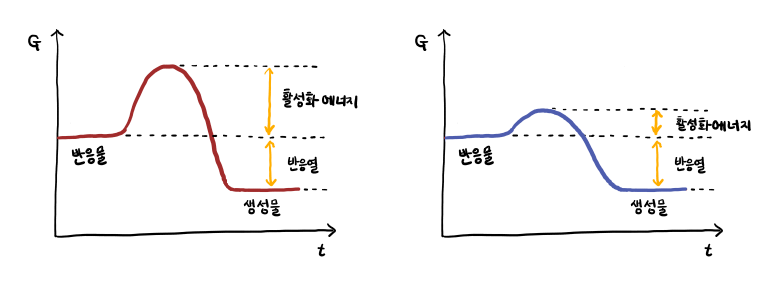
활성화에너지란 반응물이 화학반응을 하기 위해(전이상태로 전환되기 때문에) 필요한 에너지로 효소는 좌적색 그래프를 우청색 그래프처럼 활성화에너지를 낮춰 반응을 촉진하는 촉매 역할을 하는 물질이다.
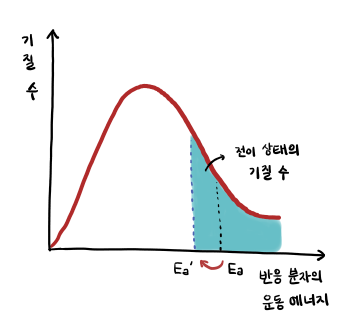
위 그래프는 반응 분자의 운동 에너지 당 기질의 수를 나타낸 것이다.그래프가 x축으로 하는 넓이는 전이 상태의 기질 수를 의미한다.효소를 처리하여 활성화 에너지가 Ea에서 Ea’로 감소하면 그래프가 x축으로 하는 넓이도 증가한다(=전이 상태의 기질 수가 증가함).
효소는 단백질이며 온도와 pH에 의해 활성이 크게 달라져 효소별로 최적의 온도와 최적 pH를 가진다.대부분의 소화효소, 가수분해효소는 단백질로만 구성된 반면 보조인자라는 비단백질이 붙어야 비로소 활성을 나타내는 효소도 있다. (이 경우 단백질 부분은 주효소라고 한다.) 보조인자에는 Fe2+, Cu2+ 등의 금속이온과 NAD+, NADP+ 등의 보효소가 있다. 이들이 주효소와 공유 결합한 것을 보결분자단이라고 한다.
*효소의 작용원리
효소(E)에 결합하는 물질을 기질(S)이라고 한다.효소는 기질과 특이하게 결합하여 효소-기질복합체(ES)를 형성하고 생성물(P)이 만들어지면 분리되어 다른 반응에 참여한다.
酵素효소의 종류
산화 환원 효소(oxidoreductase)e/H+를 첨가하거나 제거하는 산화 환원 반응 촉진 ex)탈수소 효소, 산화 효소, 환원 효소, SOD전달 효소(transferase)특정 기질로 다른 기질로 작용기 전달 ex)인산화 효소와 메틸화 효소와 아세 티 루화 효소 가수 분해 효소(hydrolase)물 분자를 첨가하여 화학 결합 절단 ex)말테이스(맥아당+H2O→, 포도당+포도당)의 분해 효소(lyase)가수 분해와 산화에 의하지 않고 기질로 원자단과 작용기를 제거하고 이중 결합 형성 ex)피루브산 탈탄산 효소(피루브산 ⇌ 아세트 알데히드+CO2)이성질체화 효소(isomerase)기질을 구성하는 원자의 위치를 바꾸어 구조적 이성체로 전환 ex)6단 댄 이성질체화 효소(포도당 6인산 ⇌ 과당 6인산)연결 효소(합성 효소)(ligase)ATP 또는 3인산뉴클레오티드로 인산기를 분해하고 방출하는 에너지를 이용하여 2가지 기질연결 ex) 구연산합성효소, 피루브산카르복실화효소
· 효소 촉매 반응에 사용되는 촉매 반응기
효소는 어떻게 기질을 전이 상태로 만드는지에 대한 내용이다 산-염기촉매: 산으로부터 H+를 전달받거나 염기에서 H+를 빼앗겨 반응을 촉진한다.② 공유결합성 촉매 : 효소가 기질과 일시적으로 공유결합을 형성하여 반응을 촉진한다.③ 금속이온촉매 : 기질의 음전하를 안정화하거나 금속이온의 산화를 이용하여 (친핵체를 생성시켜) 반응을 촉진한다.④ 접근효과 : 기질이 효소의 촉매작용기와 접촉하여 움직임을 제한하고 반응에 적절한 방향을 갖도록 결합시킴⑤ 정전기적 촉매: (정리에는 없지만 추가) 이웃한 작용기(주로 아미노산잔기)의 전하가 서로 영향을 줌으로써 기질의 전이 상태를 안정화시킬 수 있다.
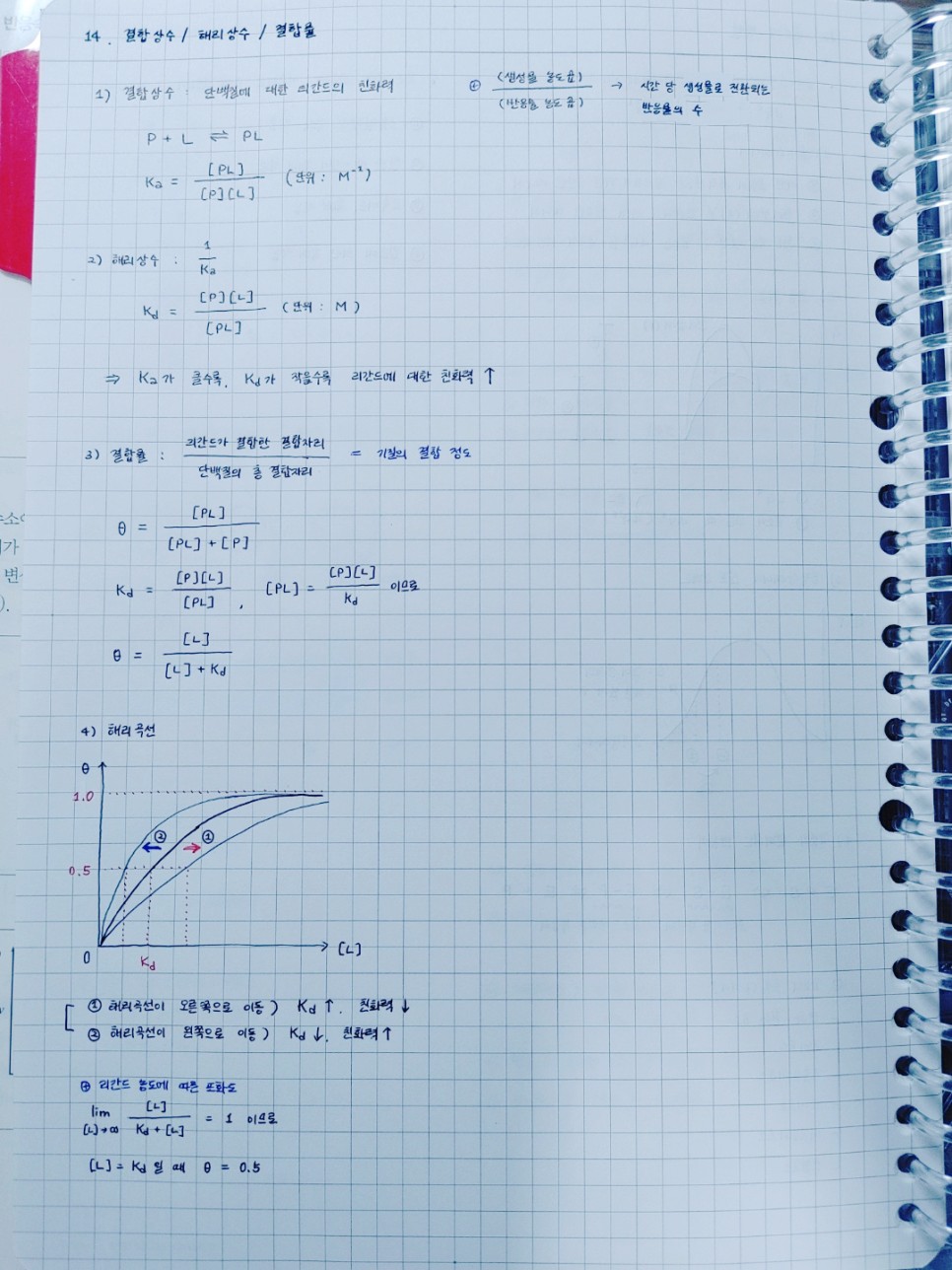
• 결합 상수/해리 상수/결합률
결합 상수는 효소에 결합하는 기질의 친화력이다. 당연히 결합상수 값이 클수록 효소에 대한 기질의 친화력은 크다.분해상수는 결합상수의 역수로 효소에서 기질이 얼마나 분리되는지를 나타내는 정수이다. 따라서 분해상수 값이 작을수록 효소에 대한 기질의 친화력은 크다. P+LPPL에서 P를 단백질(효소), L을 리간드(기질)로 하면 결합상수(Ka)와 해리상수(Kd)는 다음과 같이 구할 수 있다.기질의 친화력을 나타낼 때는 결합상수에서 분해상수(Kd)를 사용한다.
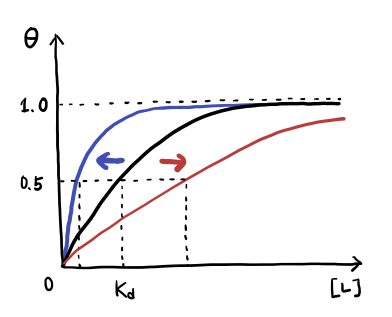
결합율은 효소의 결합좌에서 기질이 결합한 결합좌가 차지하는 비율이다.

위의 결합곡선은 이며, [ L]= Kd일 때 == 0.5이다.해리곡선이 왼쪽으로 이동하면 (청곡선) Kd값이 감소하므로 친화력이 증가한 것이고, 해리곡선이 오른쪽으로 이동하면 (적곡선) Kd값이 증가하므로 친화력이 감소한 것이다.